В.А. Волков, Е.Е. Кевер
Институт биохимической физики им. Н.М. Эмануэля РАН, Москва, Россия
Человечество всю свою историю использует растения в пищу, а также в лечебных и косметических целях. При приготовлении напитков, пищевых добавок, косметических изделий и лекарственных препаратов применяются различные технологии извлечения (экстракции) полезных веществ из тканей растений. Эти технологии различаются как по используемому экстрагенту, так и по методике экстракции и применяемому оборудованию. От методики экстракции зависит не только полнота извлечения веществ из сырья, но и степень их сохранности. Некоторые вещества (например, каротиноиды) не переносят нагрева выше 40 ͦС и действия как прямого, так и рассеянного света [1]. Другие вещества (флавоноиды, сапонины, терпеноиды) более термоустойчивы, однако для обеспечения высокого качества экстрактов проводит этот процесс при температурах выше 55 ͦС не рекомендуется. Из одного и того же сырья получаются принципиально разные по составу экстракты при использовании экстрагентов различной полярности (рис. 1 и 2).
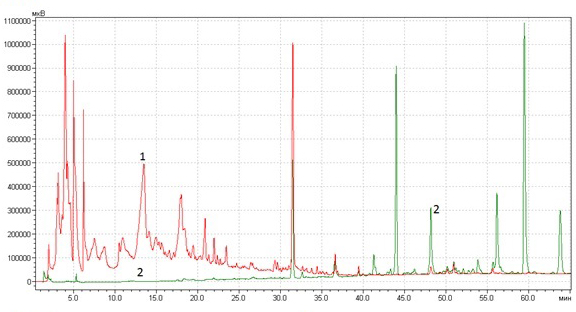
Рис. 1. Хроматограммы экстрактов ромашки: 1 – воднопропиленгликолевого, 2 - полученного с использованием сверхкритического СО2. Хроматограф Shimadzu LC-20Prominence, детектор диодно-матричный SPDM20A, колонка Merck Superspher-100 RP-18, 4x250 мм. Элюирование градиентное, элюент ацетонитрил-вода, скорость потока 0.5 мл/мин.
В левой части хроматограмм, соответствующей выходу наиболее полярных соединений, имеются пики только у воднопропиленгликолевого экстракта, в то время как в правой части, соответствующей выходу малополярных соединений – только у СО2 – экстракта.Аналогичная картина наблюдается и при сравнении воднопропиленгликолевых и масляных экстрактов:
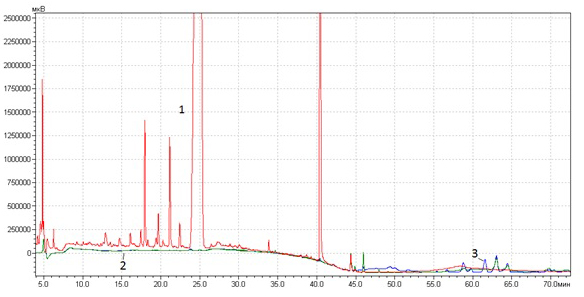
Рис. 2. Хроматограммы экстрактов календулы: 1 -воднопропиленгликолевого (Завод эндокринных ферментов, Россия), 2 - масляного экстракта (Завод эндокринных ферментов, Россия), 3 - масляного экстракта (Symrise, Германия).
Очень хорошими экстрагентами, извлекающими из тканей растений как гидро-, так и липофильные соединения, являются водно-этанольные смеси. Они с успехом применяются для производства экстрактов для приема внутрь и обработки полости рта, однако практически не применяются при производстве косметики из-за негативного воздействия на кожу и способности расслаивать косметические составы.
Поэтому для производства косметики применяются, главным образом, пропиленгликолевые и воднопропиленгликолевые экстракты. 1,2-пропиленгликоль является веществом, разрешенным для наружного и внутреннего применения, безопасность которого доказана многочисленными исследованиями. 1,2-пропиленгликоль при нанесении на кожу улучшает проникновение в нее действующих веществ косметических композиций.
Глицерин также является полностью биосовместимым веществом, более дешевым, чем 1,2-пропиленгликоль, однако, из-за высокой вязкости уступает последнему по экстрагирующей способности.
Сверхкритический (при давлении около 25 МПа) CO2 обладает превосходной способностью извлекать из тканей растений липофильные соединения в условиях максимального их сохранения, в результате чего получаются экстракты, не содержащие растворитель. Однако, гидрофильные соединения, среди которых многие ценные вещества, в частности, флавоноиды, таннины, углекислота не экстрагирует. Кроме того, такие экстракты имеют высокую себестоимость. Поэтому для извлечения жирорастворимых соединений чаще всего применяют экстракцию растительными маслами.
При использовании одного и того же экстрагента получаемые экстракты могут сильно различаться по составу и количеству экстрагированных веществ. При этом играют роль следующие факторы:
- сорт, место произрастания сырья, почвенно-климатические условия, время его заготовки;
- соблюдение технологии заготовки и хранения растительного сырья;
- метод экстракции, соотношение массы сырья и экстрагента.
На рис. 3а. представлены хроматограммы полярных соединений (главным образом, полифенолов, в т.ч. флавоноидов) ромашки аптечной (Chamomilla recutita L.), произведенных на различных российских и известном зарубежном предприятиях. Очевидно, что все экстракты изготовлены из натурального качественного сырья. Российские экстракты по величине большинства основных пиков превосходят зарубежный аналог, хотя некоторых компонентов в последнем, все же, больше, что объясняется различиями состава компонентов в исходном сырье.
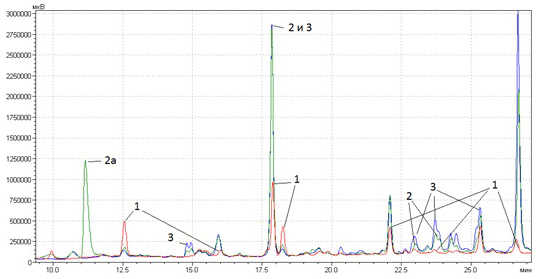
Рис. 3а. Хроматограмма полярных соединений ромашки (Chamomilla recutita L.) различных производителей: 1 – Symrise (Германия), 2 – 2Д-Фарма (Россия), 3 – Завод эндокринных ферментов (Россия).
Такая же картина наблюдается и на хроматограмме малополярных соединений ромашки:
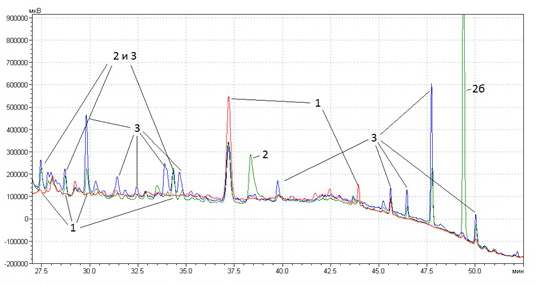
Рис. 3б. Хроматограмма малополярных соединений ромашки (Chamomilla recutita L.) различных производителей: 1 – Symrise (Германия), 2 – 2Д-Фарма (Россия), 3 – Завод эндокринных ферментов (Россия).
Иногда на хроматограммах обнаруживаются пики веществ, не входящих в состав природных композиций изучаемого экстракта (пик 2а на рис. 3а).
Однако, в некоторых экстрактах экстрактивные вещества заявленных растений обнаруживаются в очень малых количествах. В частности, нами это было выявлено при сравнительном хроматографическом анализе двух экстрактов женьшеня – известного источника тонизирующих веществ, главными из которых являются гликозилированные формы сапонинов (рис. 4):
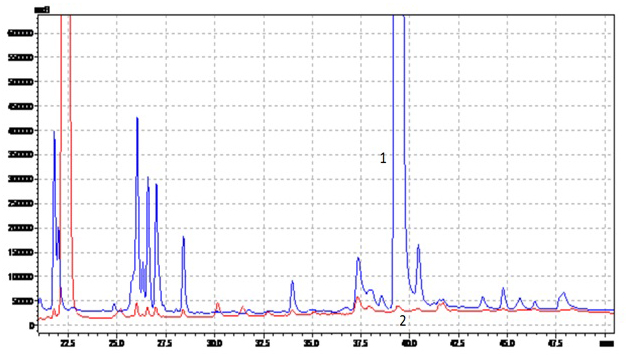
Рис. 4. Хроматограммы воднопропиленгликолевых экстрактов женьшеня различных производителей: 1 –Завод эндокринных ферментов (Россия), 2 – известная британская фирма. Пик 39.5 мин в экстракте 1 – консервант триклозан, пик 22.5 мин в экстракте 2 – консервант метилпарабен.
Экстракты растений (за исключением некоторых, содержащих сильнодействующие и ядовитые вещества), обладают высокой биосовместимостью, полинаправленностью действия и влияют на организм человека подобно внутренним метаболитам, чем обусловливается популярность использования растительных экстрактов в пищевой технологии, косметологии и медицине[2].
Со времени открытия т.н. «французского парадокса» [3] (обусловленный потреблением большого количества растительных антиоксидантов с пищей низкий уровень заболеваемости сердечно-сосудистыми заболеваниями при высоких факторах риска во Франции) ученые, промышленники и потребители стали проявлять возрастающий интерес к антиоксидантным свойствам пищевой, косметической и фармацевтической продукции. Слово «антиоксидант» превратилось из предложенного учеными ИХФ РАН Н.М Эмануэлем и Е.Б. Бурлаковой научного термина в популярный рекламный «бренд», эффективно повышающий продажи товаров и услуг, но далеко не всегда добросовестно и обоснованно используемый.
В 2004 году Главным санитарным врачом РФ утверждены «Рекомендуемые уровни потребления пищевых продуктов и биологически активных веществ» [4], в соответствии с которыми введены адекватные и верхние допустимые уровни суточного потребления АО растительного происхождения. Суммарное адекватное потребление фенольных АО составляет около 500 мг, верхнее допустимое – около 1100 мг. В США наиболее распространена точка зрения, что суточная норма потребления фенольных АО с пищей составляет около 1000 мг; при этом лишь 30% жителей США потребляют АО в количестве, соответствующем этой норме.
Тем не менее, большинство производителей пищевой и косметической продукции, использующие слово «антиоксидант» в рекламных целях, не имеют данных даже об общем количественном их содержании в исходном сырье и в готовой продукции.
В ходе наших более ранних исследований [5] мы установили на примере серии образцов белых и красных вин, что при количественном анализе общего содержания антирадикальных АО в объектах растительного происхождения наиболее адекватные результаты в сочетании с удобством применения дают методы, основанные на наблюдении инициированной люминесценции люминола и ДФПГ-тест. Последний был использован авторами данной работы и для количественного анализа содержания АО в экстрактах образцов тех же растений, в отношении экстрактов которых был ранее проведен хроматографический анализ.
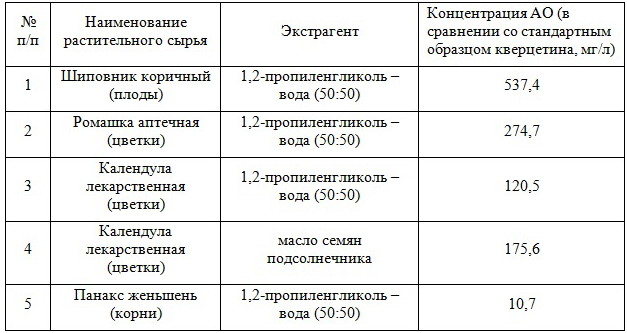
При анализе суммарной концентрации АО в образцах некоторых отечественных экстрактов, производимых для нужд косметической промышленности (Завод эндокринных ферментов, Москва, см. таблицу) было установлено, что экстракты надземных частей растений содержат АО в количестве, равном их содержанию в высококачественных красных виноградных винах [6]. Тот факт, что масляный экстракт календулы лекарственной содержит АО значительно больше, чем воднопропиленгликолевый, объясняется присутствием в исходном подсолнечном масле значительного количества токоферолов и токотриенолов, главным образом, α-токоферола, которые обеспечивают большую часть наблюдаемой антиоксидантной активности масляных экстрактов.
Экстракты подземных частей растений, в частности, женьшеня, содержат гораздо меньше АО, чем экстракты надземных частей. Тонизирующее действие этого экстракта связано, главным образом, с гликозидами сапонинов [2], которые имеют стероидную химическую природу и антиоксидантными свойствами не обладают.
Таблица. Суммарная концентрация АО в образцах некоторых воднопропиленгликолевых и масляных экстрактов, производимых для нужд косметической промышленности (Завод эндокринных ферментов)
Таким образом, для обеспечения высокого качества продукции на основе растительного сырья и ее конкурентных преимуществ предприятиям необходимо при отборе поставщиков и выборе производственных технологий осуществлять контроль физико-химических параметров экстрактов и конечного продукта с применением современных аналитических методов, дающих адекватные представления об их свойствах. Проведенные исследования продемонстрировали, что производство экстрактов в странах Европейского Союза не является показателем их качества, и имеются превосходящие их российские аналоги.

